Soient n1 moles d’un gaz parfait G1 dans un volume V1 et n2 moles d’un gaz parfait G2 dans un volume V2 juxtaposé, sous la même pression P1 = P2 et la même température T1 = T2, l’ensemble constituant un système isolé (voir Figure ci-dessous).
On retire la cloison qui les sépare et on suppose que le mélange des gaz ainsi réalisé est idéal ie : les interactions entre les molécules de G1 et G2 sont négligées.
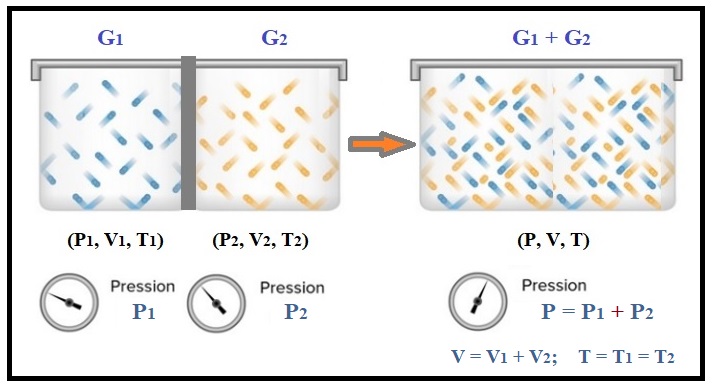
1-) Exprimer les pressions partielles de G1 et G2 dans le mélange, respectivement P1 et P2, en fonction de P, V1 et V2.
2-) Effectuer un bilan entropique (variation d’entropie du mélange) en fonction de n1, n2 et R
3-) Commenter le signe de cette variation d’entropie.
4-) Calculer la variation d’entropie du mélange pour V1 = V2 = 1 litre; P = 3bar et T = 18K.
