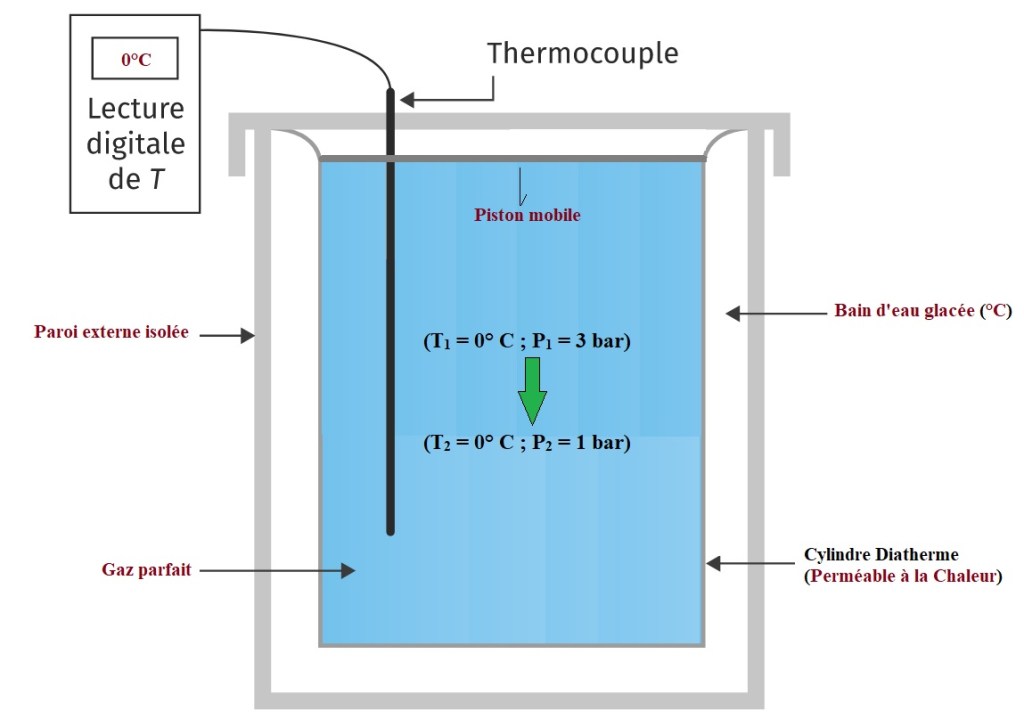
Un cylindre diatherme fermé par un piston constitue un système perméable à la chaleur. Il contient une mole de gaz parfait dans l’état initial T1 = 273 K ; P1 = 3.105 Pa. Ce système est plongé dans un bain d’eau-glace constituant un Thermostat à 0°C (273 K). On agit sur le piston mobile pour détendre réversiblement le gaz jusqu’à P2 = 105 Pa. On donne R = 8,315 SI.
1-) Rappeler l’unité de la constante R dans les unités du Système International.
2-) Déterminer la masse de la glace apparaissant das le Thermostat. La chaleur latente massique de fusion est Lf = 334 J.g-1
3-) Calculer la variation d’entropie du gaz et celle du Thermostat. Que peut-on dire de l’entropie créée ?

J’adore 💕 merci beaucoup. Votre Blog nous aide énormément
J’aimeJ’aime