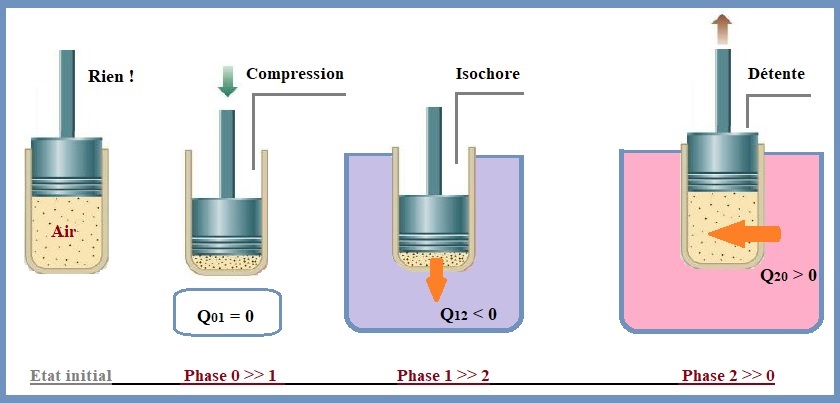
Un cylindre, fermé par un piston mobile sans frottement, contient n moles d’air gazeux, considéré comme gaz parfait diatomique (voir figure ci-dessous). Le cylindre étant un très bon conducteur, le gaz est en contact thermique avec le milieu ambiant à la température T0 = 300K, ce dernier jouant le rôle de thermostat. On fait décrire à ces n moles d’air un cycle constitué par les trois transformations suivantes :
-a) Une compression adiabatique réversible au cours de laquelle le contact thermique avec le milieu ambiant est supprimé : le gaz passe de l’état 0 (P0 = 1bar ; V0 = 1,2L ; T0 = 300K) à l’état 1 (P1; V1 ; T1) qui triple sa pression ;
-b) Un refroidissement isochore au contact du milieu ambiant, de façon à revenir à la température T0 dans l’état 2 (P2 ; V2 ; T2 = T0) ;
-c) Une détente isotherme réversible au contact du milieu ambiant qui le fait revenir à l’état initial 0.
1°) Rappeler l’expression de la première Identité Thermodynamique ainsi que son domaine de validité.
2°) Qualifier, d’un point de vue entropique, la transformation de 0 à 1.
3°) En déduire (une démonstration est exigée) la relation qui relie les températures et volumes des états 0 et 1.
4°) Démontrer que V1 = 0,55L et T1 = 410K.
5°) Calculer les variations d’entropie du gaz ΔSi-j pour chaque transformation ouverte i – j du cycle. Commenter chaque signe.
6°) Vérifier sur ce cycle que l’entropie est une fonction d’état.
7°) Calculer Qcycle.
8°) Un tel cycle caractérise une machine thermique monotherme, s’agit-il d’un moteur ou d’un récepteur ? Vous pourriez commenter à l’aide de l’énoncé de Kelvin, du 2nd Principe de la Thermodynamique.
9°) Vérifier que ce cycle décrit une transformation fermée irréversible.
