Note Culturelle :
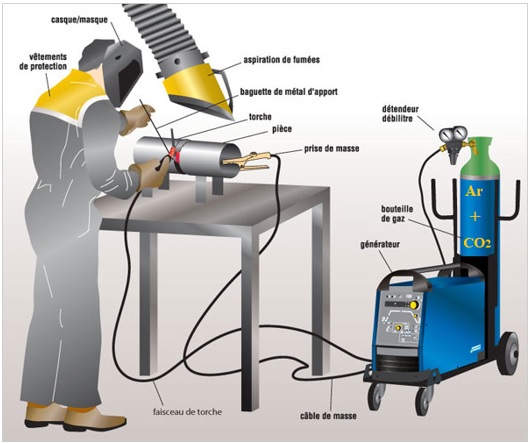
L’argon est utilisé dans la fabrication de l’acier où il empêche l’interaction entre le métal liquide et l’atmosphère environnante. Il est également utilisé dans l’électronique et la fabrication de pièces automobiles. Les bouteilles d’argon pur et d’argon sous forme de mélange (Ar + CO₂) sont couramment utilisées dans les procédés à l’arc électrique pour la soudure de l’aluminium, de l’acier – carbone et de l’acier – inox, du bronze et du cuivre (voir figure ci-dessous). Lorsqu’il est utilisé comme gaz d’appoint dans les applications de soudage à l’arc, d’injection de gaz ou de découpage au plasma, l’argon fournit une atmosphère inerte qui empêche l’oxydation ou d’autres réactions chimiques nuisibles au soudage et réduit les émissions.
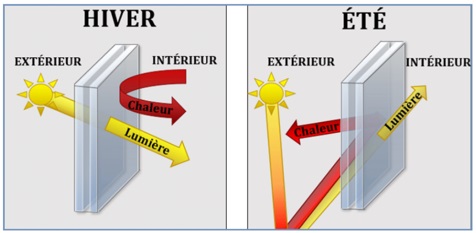
L’argon fait également partie des gaz les plus couramment utilisés par les constructeurs de fenêtres, afin d’optimiser l’isolation des fenêtres double vitrage. La plupart du temps, les constructeurs procèdent par injection pour introduire le gaz entre les vitrages. Ce procédé va empêcher les déperditions de chaleur en hiver et diminuer le rayonnement solaire pénétrant dans les habitations en été.
L’objectif de cet exercice est de déterminer la variation d’entropie d’un système (argon gazeux), subissant un processus pas forcément adiabatique, ni isotherme, ni isobare et encore moins isochore. Pour cela, une mole d’argon à l’état gazeux (gaz parfait monoatomique) est mise en contact avec un réservoir de chaleur qui le conduit très lentement de l’état initial (V0, P0 = 1atm), à l’état final où son volume a été réduit de moitié (V1 = V0/2, P1 = 4atm). Le gaz et le réservoir sont enfermés dans une enceinte parfaitement calorifugée.
On donne : cp = 5R/2 et cv = 3R/2 ; avec R = constante des gaz parfaits ; MAr = 40 g/mol, masse molaire de l’argon.
1-) Quelle hypothèse fait-on en précisant que la transformation subie par le gaz est très lente ? en déduire les implications sur la variation d’entropie de l’univers (gaz + réservoir).
2-) Si la transformation avait été brutale (très rapide), quelles auraient été les implications sur la variation d’entropie de l’univers (gaz + réservoir).
3-) Déterminer l’exposant adiabatique ou constante de Laplace de l’argon γ.
4-) Exprimer la variation d’entropie du gaz ΔSgaz en variable (P,V) et en fonction de m, cv et γ.
5-) Calculer alors ΔSgaz et en déduire la variation d’entropie du réservoir ΔSréservoir.
